Разработка учебных занятий в средней и высшей школе
Химические свойства белков
Учитель химии. Химические свойства белков определяются строением и характером радикалов. Именно радикалы обеспечивают исключительное разнообразие химических реакций белков и оказывают существенное влияние на их функциональную активность.
Ученик (сообщение). Одним из общих свойств белков является гидролиз. Гидролиз происходит при нагревании белков с растворами кислот или щелочей или при действии ферментов. Конечный продукт гидролиза – аминокислоты. Так, полный гидролиз одного трипептида приводит к образованию трех аминокислот. (Демонстрируется схема гидролиза, рис. 8.)
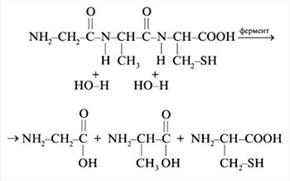
Рис. 8. Схема гидролиза трипептида
Гидролиз белков сводится к расщеплению полипептидных связей. Таким же образом происходит и переваривание белков. Во время пищеварения белковые молекулы гидролизуются до аминокислот. Аминокислоты хорошо растворимы в водной среде, они проникают в кровь и поступают во все ткани и клетки организма.
Здесь большая часть аминокислот расходуется на синтез белков различных органов и тканей, в том числе гормонов, ферментов и других биологически важных веществ, а остальная часть – на энергию.
Учитель химии. Белки, как и другие вещества, можно узнать с помощью качественных реакций.
Учащиеся проводят лабораторные опыты – цветные качественные реакции на полипептиды.
Опыт 3. Биуретовая реакция
К 2–3 мл раствора белка в пробирке добавьте 2–3 мл 10%-го раствора гидроксида натрия. К полученной смеси прилейте 2–3 мл раствора сульфата меди(II). Пробирку встряхните и наблюдайте изменение цвета.
Опыт 4. Ксантопротеиновая реакция
В пробирку налейте 2 мл раствора белка и добавьте по каплям 0,5 мл концентрированного раствора азотной кислоты. Осторожно нагревайте пробирку и наблюдайте изменение цвета.
Опыт 5. Обнаружение белка в мясном бульоне
Поместите в пробирку кусочек мяса и залейте его водой. Нагрейте пробирку до температуры кипения воды и 2–3 мин кипятите содержимое (тем самым получите бульон).
Отфильтруйте бульон через марлю с помощью воронки в другую пробирку. Определите наличие белка в бульоне с помощью биуретовой и ксантопротеиновой реакций. Сделайте вывод.
Опыт 6. Обнаружение натуральной шерсти
Подожгите шерстяную нить. Сделайте вывод о признаках горения.
Ученик (сообщение). Из биологии известно, что многие белки имеют спиральную вторичную структуру. Другой пример вторичной структуры – в виде гармошки (![]() -структура, рис. 9).
-структура, рис. 9).
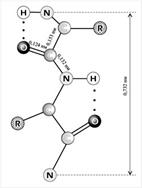
Рис. 9. Вторичная структура белка в виде гармошки
Структуру поддерживает сила взаимодействия между карбонильным кислородом (С=О) и атомом водорода при азоте – водородная связь. Водородная связь противостоит тепловому движению звеньев, стремящемуся разорвать эту структуру.
Учитель химии. Что же происходит при повышении температуры? Из курса физики 10-го класса мы знаем, что температура – величина, характеризующая интенсивность движения атомов. Температура прямо пропорциональна среднеквадратичной скорости атомов и среднекинетической энергии (Е = m![]() 2/2 = 3/2kT). Поэтому повышение температуры (увеличение внутренней энергии движения) вызывает увеличение амплитуды колебаний атомов звеньев структуры. Следовательно, увеличивается расстояние между атомами, связываемыми водородной связью. При больших амплитудах колебаний водородная связь разрушается, при этом увеличивается нагрузка на соседние связи спиральной структуры, и в конечном итоге структура белка быстро распадается (рис. 10).
2/2 = 3/2kT). Поэтому повышение температуры (увеличение внутренней энергии движения) вызывает увеличение амплитуды колебаний атомов звеньев структуры. Следовательно, увеличивается расстояние между атомами, связываемыми водородной связью. При больших амплитудах колебаний водородная связь разрушается, при этом увеличивается нагрузка на соседние связи спиральной структуры, и в конечном итоге структура белка быстро распадается (рис. 10).
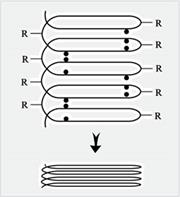
Рис. 10. Разрушение вторичной структуры белка при нагревании
Молекула после разрушения связей тоже «расползается», она больше не может противостоять хаосу теплового движения. Вступает в действие механизм внутренней подвижности – повороты звеньев вокруг валентных связей цепи. Макромолекула приобретает новую конфигурацию (она сворачивается в клубок – как бы плавится). Изменяя температуру в обратном направлении, т. е. понижая степень хаоса, можно вновь получить макромолекулу исходной структуры.
Еще по теме:
Дифференциация младших школьников с ЗПР по группам
Для разработки рекомендаций по совершенствованию коррекционно - развивающего обучения младших школьников с задержкой психического развития было проведено исследование, позволившее дать подробное дифференцированное описание психолого - педагогических особенностей участников исследования. В результат ...
Требования к представлению информации на слайде
Работа с визуальной информацией, подаваемой с экрана, имеет свои особенности, может вызвать утомление, снижение остроты зрения. Особенно трудоемкой для человеческого зрения является работа с текстами. Вследствие этого при создании слайдов необходимо учесть целый ряд требований. 1. Содержание информ ...
Виды чтения
Вопрос о видах чтения в настоящее время является наиболее разработанным и одновременно терминологически наименее устоявшимся. В исследованиях ученых мы можем найти много названий видов чтения. Их огромное количество можно объяснить тем, исследователи предлагают самые разные классификации видов чтен ...
Педагогика как наука

Обучение было и всегда будет, пока живет человечество. Можно сказать, что подготовка молодого поколения к участию в жизни общества путем передачи социального опыта есть неотъемлемая общественная функция во все времена и у всех народов.
Категории
- Главная
- Методы производственного обучения
- Новые технологии обучения
- Обучение чтению на начальном этапе
- Сущность воспитания
- Информатика и образование
- Формирование деятельности
- Карта сайта
